没学会原子物理,试着重新看ppt搞一下复习。
🤩小目录🤩
第0章 原子物理学要回答的问题是
原子结构是什么样子的
原子为什么可以稳定存在
第1章 原子的核式模型
背
\[\begin{aligned} & e = 1.60\times 10^{-19}C\\ & m_e = 9.11\times 10^{-31}kg\\ & m_p = 1.67\times 10^{-27}kg\\ & \frac{m_p}{m_e} = 1836 \end{aligned}\]1.1 电子的发现
历史的回顾:原子论
道尔顿——化学元素由原子组成,无法进一步分割。同种元素的原子相同,不同元素的原子不同;倍比定律。
阿伏伽德罗:分子是决定物质性质的最小微元。原子-分子学说
1.1.1 汤姆孙实验
电子的发现,荷质比的测定。
阴极射线管
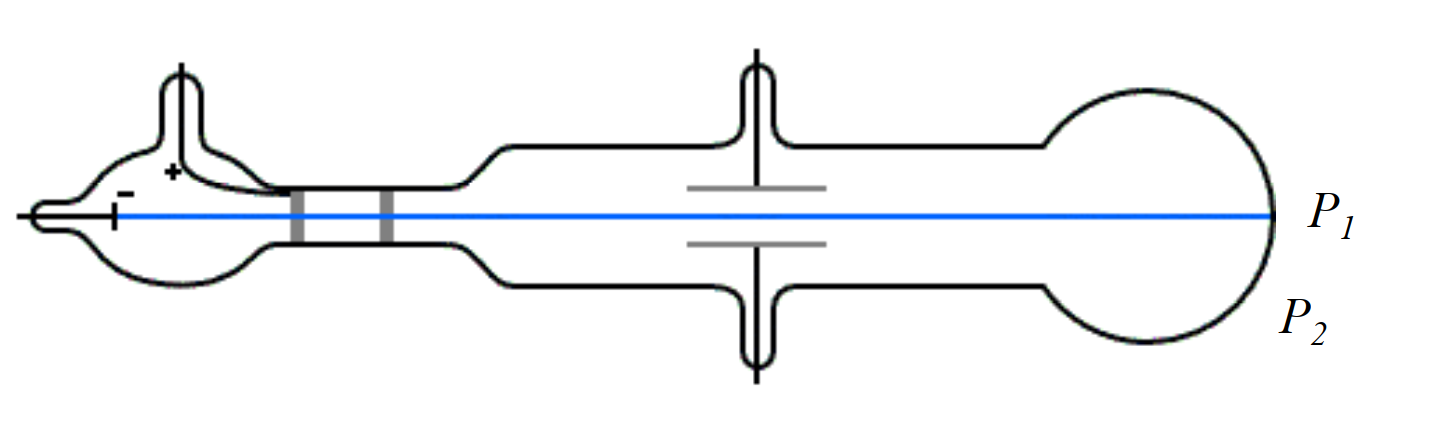
(1)加电场:向下偏转——阴极射线带负电;
(2)加磁场,去电场:圆形轨迹——能算出荷质比$\frac{e}{m}=1.76\times 10^{11}C/kg$
1.1.2 密里根油滴实验
元电荷的测定。
1.2 原子的核式模型
也就是卢瑟福模型。
1.2.1 汤姆孙的原子模型
又叫枣糕模型、西瓜模型。
内容:原子中的正电荷均匀分布在整个原子球体内,而电子则嵌在其中。
盖革-马斯顿实验表明,汤姆孙模型是错误的。
1.2.2 盖革-马斯顿实验
内容:用α粒子轰击金箔,发现大多数α粒子发生约1°的偏转,但有$\frac{1}{8000}$的概率发生大角度偏移。
如果是汤姆孙模型?产生90°偏移的概率为$10^{-3500}$。(与实验结果不符)
1.2.3 库仑散射偏角公式
单次散射,只考虑库仑作用,忽略核外电子,靶核静止。
- 库仑散射公式
其中,b为瞄准距离,a为库仑散射因子,是一个常数,$\theta$为偏转角。
- 库仑散射因子
其中,$Z_1,Z_2$分别为α粒子和原子核的电荷数,$E$为α粒子具有的能量(动能?势能?两者之和?)。
1.2.4 卢瑟福散射公式
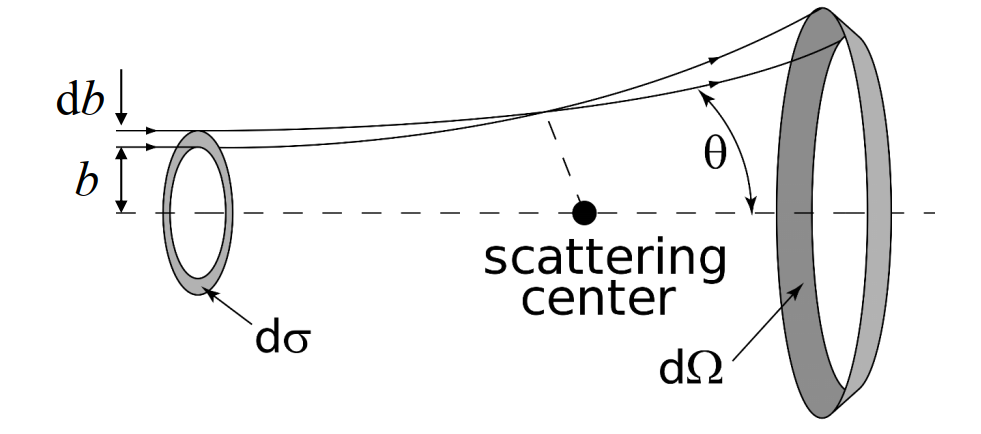
微分散射截面:
\[\sigma_c(\theta)=\frac{d\sigma}{d\Omega}=\frac{a^2}{16\sin^4\frac{\theta}{2}}\]设入射粒子有$N$个,散射到$\theta$角方向上的有$dN’$个,则
\[\frac{dN'}{Nd\Omega }=\frac{ntd\sigma }{d\Omega}=nt\sigma_c(\theta)\]$\sigma_c(\theta)$含义:$\sigma_c(\theta)$代表对于单位面积内每个靶核,单位入射粒子,单位立体角内的粒子数。
微分散射截面也称作几率,即每个入射粒子被散射到单位立体角内的几率。
看不懂,摆!
探讨:
\[\frac{dN'}{Nd\Omega }=\frac{nta^2}{16\sin^4\frac{\theta }{2}}\]同一α粒子源:a不变;同一靶材:n,t不变。
可以据此来控制变量,设计实验,绘制曲线(线性化),检验卢瑟福公式是否正确。盖革-马斯顿后来就干了这事。
1.2.5 卢瑟福的行星模型
带正电的原子核集中在原子中心很小的区域内,带负电的电子在原子核外绕核做圆周运动。
原子核大小:$10^{-14}\sim 10^{-15}\ m$
原子大小:$\sim 10^{-10}\ m$
第2章 玻尔的氢原子理论
2.1 黑体辐射
2.1.1 卢瑟福模型的困难
- 原子的稳定性
绕核旋转的电子因具有加速度(含向心加速度)而辐射出电磁波,损失能量,进而坠入原子内。按经典理论推算,这样的原子寿命很短($\sim 10^{-10}s$),极不稳定。
- 原子的同一性
不同的初始条件会形成不同的结果,因此不可想象还会存在另一个太阳系。然而轻而易举就能找到同样的原子。
- 原子的再生性
原子与外来粒子互相作用后还会恢复原样,就像什么也没有发生过一样。很怪。
2.1.2 量子假说根据之一:黑体辐射
热辐射:分子热运动导致物体不断辐射电磁波,称为热辐射。
任何物体(含黑体)任何温度下都有热辐射,热辐射发出的电磁波是连续光谱。温度越高,辐射能越大,波长越短。
基尔霍夫热平衡定律:与外界隔绝、温度互不相同的物体不断发射和吸收热辐射,一段时间后所有物体的温度相同,达到热平衡。热平衡状态下,物体辐射能量和吸收能量相同,物体的辐射本领与吸收本领成正比,比值只与$T,\nu$有关。
黑体:能完全吸收各种波长的电磁波而无反射的物体。(有辐射)
维恩公式:高频段与实验曲线符合得很好,低频段明显偏离实验曲线。
瑞利-金斯公式:低频段与实验曲线符合得很好,高频段紫外灾难。
普朗克的黑体辐射公式:黑体空腔中的谐振子的能量不能是任意值,只能取一系列不连续的、分立值,这些值是某一最小能量($\epsilon_0=h\nu$)的整数倍。
\[E(\nu,T)=\frac{8\pi h\nu^3}{c^3}\frac{1}{e^{\frac{h\nu}{k_BT}}-1}\]2.2 光电效应
2.2.1 量子假说根据之二:光电效应
光电效应:在光的照射下物体发射电子的现象。
特征:
① 光照到金属时,电流几乎同时产生。
② 反向电压$V$和光的频率$\nu$一定时,光电流$i$与光强$I$成正比。
③ 光强$I$和光的频率$\nu$一定时,光电流$i$随减速势$V$增加而减小。
④ 对于特定表面,遏止电压$V_0$与光的强度$I$和光电流$i$无关。
2.2.2 旧理论解释光电效应的困难
根据旧理论:
① 只要光强足够大或者延长光照时间来积累能量,总可以让电子获得足够的能量,突破逸出功的限制,发生光电效应。(与瞬时性、遏止电压矛盾)
② 决定光电子能量的是光强,与频率无关。
③ 不存在阈频率。
2.2.3 爱因斯坦光量子假设
- 光量子
光量子是局限于空间某一小范围的、以光速c运动的能量子单元。电磁辐射由光量子组成。
光子能量$E=h\nu$。
光量子具有整体性,即光的发射、传播和吸收都是量子化的。
- 爱因斯坦的光量子理论
一个光子将全部能量交给电子,电子克服金属对它的束缚(逸出功:$\Phi$),从金属中逸出。
\[\frac{1}{2}m_ev_m^2=h\nu - \Phi\]当频率一定时,随光强增大,单位时间内被电子吸收的光量子旧越多,因此光电流就越大。
- 对光电效应的成功解释
光的频率$\nu$:决定了光量子的能量大小,说明电子的初动能是由频率决定的,存在遏止电压。
光强$I$:光强越大,单位时间内打出的电子就越多,光电流就越强。
瞬时性:电子一吸收光量子就立刻逸出。
阈频率:$\nu=\frac{\Phi}{h}$
- 密利根光电效应实验
调整反向电压,得到$V_{stop}-\nu$曲线,得到其斜率$K=h/e$,计算得$h=6.56\times 10^{-34}J/s$。与其他方法算得的h符合得很好。
2.3 光谱技术
- 概念
光谱:电磁辐射频率成分和强度分布的关系图。
光谱仪:将混合光按不同波长成分展开成光谱的仪器。
光谱分析:每种原子都有自己的特征谱线,因此可根据光谱来鉴别物质和确定其化学组成,这种方法叫做光谱分析。
- 光谱结构
连续光谱(固体热辐射)、线光谱(原子发光)、带光谱(分子发光)。
- 光谱机制
发射光谱、吸收光谱。
- 人物
夫琅和费:现代光谱仪
Ångström:太阳光谱,长度单位Å(埃)。
2.4 氢原子光谱
氢原子光谱的实验规律:
记n为第n条谱线,有Balmer经验公式(1885):
\[\lambda = B\frac{n^2}{n^2-4},\quad n=3,4,5\]Rydberg经验公式(1890):
\[\tilde{\nu}=\frac{1}{\lambda }=R_H\bigg(\frac{1}{m^2}-\frac{1}{n^2}\bigg)\]$R_H$称为里德伯常数。
Balmer系是Rydberg公式中m=2的特殊情形。
还有莱曼系、布喇开系等。
2.5 玻尔的氢原子模型
卢瑟福模型中,电子绕核旋转会发出电磁波,电磁波频率等于电子回转频率,发射光谱应为连续谱,且原子寿命短暂,与事实不符。
2.5.1 玻尔模型三句话
- 经典轨道加定态条件
电子只能处于一些分立的轨道上,并且只能在这些轨道上绕核运动。不辐射电磁波,能量稳定。按经典理论,其能量为
\[E_n=-\frac{1}{2}\frac{e^2}{4\pi \epsilon_0r_n}\quad n=1,2,3,...\]定态:电子在特定的轨道绕着原子核稳定旋转。
- 频率条件
当电子从一个定态轨道跃迁到另一个定态轨道时,会以电磁波的形式放出或吸收能量$h\nu$,其值由能级差决定:
\[h\nu = E_m-E_n\]由能级定态得到轨道定态:
\[\left. \begin{aligned} E_n=-\frac{1}{2}\frac{e^2}{4\pi \epsilon_0r_n}\\\\ E_n=-hc\frac{R_H}{n^2} \end{aligned} \right\}r_n=\frac{1}{4\pi \epsilon_0}\frac{e^2}{2R_Hhc}n^2\]- 角动量量子化假设
里德伯常数的推导:
当$m,n\to \infty$时,考虑近邻跃迁$m-n=1$,得到
\[\nu=R_Hc\bigg(\frac{1}{n^2}-\frac{1}{m^2}\bigg)\approx R_Hc\frac{2}{n^3}\]又,$n\to \infty$时,量子论回归经典形式
\[\nu = \frac{v}{2\pi r}=\frac{e}{2\pi }\sqrt{\frac{1}{4\pi \epsilon_0m_er^3}}\]由此可计算出$r_n$,与上一部分得到的$r_n$联立可解得$R_H$:
\[R_H=\frac{2\pi^2e^4m_e}{(4\pi\epsilon_0)^2ch^3}\]代回$r_n$,得到角动量量子化:
\[L=m_er_nv_n=\sqrt{\frac{m_ee^2r}{4\pi\epsilon_0}}=n\hbar\]其中$\hbar=\frac{h}{2\pi}$。
角动量量子化来自电子的波动性:首尾位相相同的环波才能稳定存在。
2.5.2 一些数字
精细结构常数:
\[\alpha=\frac{e^2}{4\pi\epsilon_0\hbar c}\approx\frac{1}{137}\]玻尔半径与定态轨道半径:
\[a_0\approx 0.53Å\\\ \\ r_n=n^2a_0\]基态能量与定态轨道能量:
\[E_1=-13.6eV\\\ \\ E_n=\frac{E_1}{n^2}\]光谱项:
\[T_n=\frac{R_H}{n^2}=-\frac{E_n}{hc}\\\ \\ \Rightarrow E_n=-\frac{hcR_H}{n^2}\]2.5.3 修正
- 原子核质量有限带来的修正
两体问题:绕质心旋转+约化质量。
约化质量:
\[\mu=\frac{m_1m_2}{m_1+m_2}\]- 相对论修正
质量与速度相关:
\[m=\frac{m_0}{\sqrt{1-\frac{v^2}{c^2}}}\]2.5.4 氘、类氢离子、里德堡态
- 氘
D,由光谱分析发现。诺贝尔奖。
- 类氢离子
核外只有一个电子而核内有多于一个正电荷的原子体系,如He+,Li2+等。
玻尔的类氢离子理论:核电荷$e\to Ze$。
比克林从星光中发现了类巴耳末系,$R$与$R_H$略有不同。证明是He+。
- 里德堡态
原子或分子中电子被激发到高量子态的情况。
2.5.5 弗兰克-赫兹实验
成就:确认了原子经电子碰撞后吸收能量的分立性(原子内部能量量子化,存在能级),验证了玻尔模型。
电子通过与原子碰撞失去能量。失去的能量是量子化的,因此检测到的电流会有数个峰值。
2.5.6 索末菲的椭圆轨道
发现氢的$H_{\alpha}$线是双线。索末菲将圆形轨道修改为椭圆轨道来弥补玻尔理论的不足。
2.5.7 成就与困难
- 成就
- 第一次把光谱的实验事实纳入一个理论体系中。
- 提出动态的原子结构轮廓;指出经典理论有的不适用于原子内部。
- 提出了微观体系特有的量子规律。
- 困难
不能推广至氦及之后的原子。
谱线问题。
Now you’re a quantum physicist!